以抗PD-L1为代表的免疫治疗备受各界关注。Atezolizumab(anti-PD-L1)已被FDA批准用于阳性转移性三阴性乳腺癌(TNBC)适应症的治疗。对早期乳腺癌有预后预测方法上,目前主要依靠于H&E间质肿瘤浸润淋巴细胞(sTIL)评分和 PD-L1(SP142)免疫组化检测。但PD-L1(SP142) 检测高度赖于操作者,在临床研究中不足以精确地描述sTILs/PD-L1的动态变化。
Page教授的研究团队近期在《Breast Cancer Research》上发表了题为《Multiplex immunofluorescence to measure dynamic changes in tumor-infiltrating lymphocytes and PD-L1 in early-stage breast cancer》的文章,讨论了多重免疫荧光(mIF)与统计建模相结合,如何从单一石蜡包埋的载玻片中精确估计sTIL评分、PD-L1表达和其他免疫变量的动态变化,从而全面表征新型免疫治疗药物的活性,克服传统方法中对操作和判读的高度依赖性。
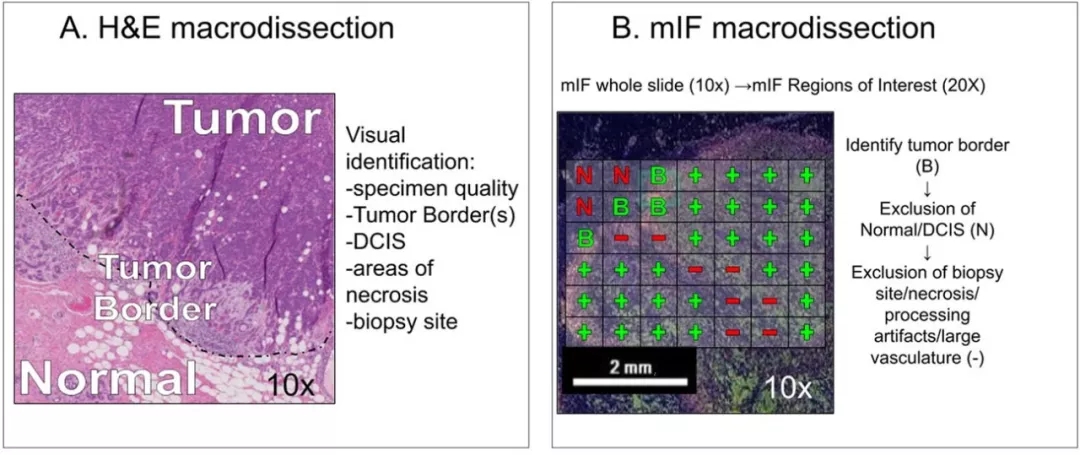
研究人员从近期临床实验(NCT02950259)获得了一系列组织样本,评估了局部区域细胞因子刺激作为一种策略促进免疫细胞浸润和激活抗乳腺肿瘤免疫的有效期。研究过程中,通过mIF (Phenoptics多色免疫荧光方案)分析治疗前的活组织检查样本和治疗后的肿瘤切除样本,标记了组织中的肿瘤细胞(cytokeratin)、免疫细胞(CD3、CD8、CD163、FoxP3)和PD-L1表达细胞。同时,对比了mIF评估sTIL评分和PD-L1表达的估计与H&E/SP142检测结果的一致性。

mIF能够在高倍放大区域(以下称为感兴趣区域,ROI)的高分辨率下估算免疫细胞计数,对多个表型表面标记,实现单个细胞的表型定义及定量,能更准确、更精确的描绘sTILs和PD-L1表达细胞并定量评估。mIF还可以对细胞进入不同组织腔室(即肿瘤与基质)的空间定位进行观察和分析,更详细地揭示免疫细胞和肿瘤细胞之间的相互作用。

mIF对sTIL和PD-L1表达的估计与传统的HE/SP142检测结果密切相关。在与临床试验一致的基础上,mIF有助于更客观地、更精确地量化与治疗相关的sTILs/PD-L1的动态变化。结合分层线性建模,可以减轻肿瘤内异质性对免疫细胞计数估计的影响,在临床试验中更有效地检测与治疗相关的药效学效应。
多色免疫荧光技术优势小结
简而言之,结合RING研究的汇总,作者提出mIF可用于ESBC I-O试验,帮助更有效地检测ICs和PD-L1表达与治疗相关的动态变化。
避免H&E结果评估中将非淋巴细胞或上皮内TILs误分类为sTILs。mIF通过使用多种细胞表面标记物对淋巴细胞进行精确分类,可以大大减少这种错误的发生。
不同评估者在用H&E量化sTILs时,使用不同的设定点/量表,导致观察者之间存在不一致。mIF可以实现流程标准化,一旦各机构之间的染色、成像和分析工作流程变得一致,这一问题也可以得到解决。美国国立卫生研究院癌症免疫监测和分析中心(CIMAC)正在努力标准化和验证mIF工作流程。
肿瘤各区域的sTILs计数的异质性产生的误差。减少这种错误的一个建议解决方案是在多个ROI中采样并平均sTILs计数结果。